Los avances científicos en materia de trasplantes en humanos de órganos modificados genéticamente y provenientes de cerdos, se han convertido en los últimos años en una esperanza de vida, pero también han generado importantes dilemas éticos.
Ante la cantidad de personas que mueren cada año sin tener acceso a un órgano donado, una opción como esta representa, sin duda, un futuro prometedor. Sin embargo, alterar genéticamente a un ser vivo genera, además, muchas dudas.
Las dudas crecen más cuando se trata de crear órganos humanos directamente en embriones de cerdo, tal como hizo el equipo a cargo de la creación de Quimera, un tejido híbrido generado en fetos de cerdo modificados genéticamente.
No menos preguntas generan los xenotrasplantes, como se denomina a los que provienen de otras especies, con años de desarrollo y pruebas medianamente exitosas, que implican alterar genéticamente a los cerdos donadores para que sus órganos no generen rechazo en el humano receptor.
Quimera

El primer esbozo de un órgano humano en embriones de cerdo fue creado por un equipo de científicos chinos y un médico español. Se trata de un tejido híbrido denominado Quimera, en referencia al animal mitológico con cabeza de león, vientre de cabra y cola de dragón.
Esta investigación – que provoca tanto esperanzas como dilemas éticos para la medicina moderna – fue publicada recientemente en la revista científica Cell Stem Cell. Se desarrolló bajo el liderazgo del científico chino Liangxue Lai, continuando el estudio del español Juan Carlos Izpisúa, quien en 2017 anunció la creación de embriones de cerdo-humano con una célula humana por cada 100.000 porcinas. En ese momento, un comité de expertos autorizó los ensayos, exigiendo que ningún animal con células humanas pudiera reproducirse.
Para llevar adelante la investigación el equipo del Instituto de Biomedicina y Salud de Guangzhou de China reprogramó células humanas adultas, con el objeto de recuperar su capacidad de formar cualquier órgano o tejido del cuerpo. Luego, éstas fueron introducidas en embriones de cerdo de pocos días, modificados genéticamente para no desarrollar riñones porcinos.
De esta manera, las células humanas se instalaron en la zona y formaron un riñón rudimentario, que consiste en una fase intermedia del sistema renal, conocida como mesonefros. Los embriones fueron gestados en cerdas hasta los 28 días, lo que representa una cuarta parte del tiempo de gestación de la especie.
Un gran paso

Josep Maria Campistol, nefrólogo y director general del Hospital Clínic de Barcelona, aunque aún no se ha logrado desarrollar órganos humanizados en cerdos, el estudio “demuestra que las células se pueden organizar en el espacio y dar lugar a estructuras tisulares organizadas, lo que representa un gran paso adelante”.
Diversos especialistas consideran que los embriones de cerdo-humano podrían convertirse en “una fuente inagotable de órganos, con la posibilidad, además, de generar órganos humanos específicos, personalizados, para determinados pacientes”, y también una oportunidad para conseguir el recambio de células de una persona concreta. “Estoy convencido de que, en un futuro próximo, vamos a ser capaces de regenerar los riñones, los hígados o los corazones que estén enfermos crónicamente, para restablecer total o parcialmente su función y evitar el trasplante”, dijo Campistol, quien es uno de los coautores de la investigación liderada por Izpisúa.
Por tratarse del primer órgano creado dentro de otro animal, existen diversos dilemas éticos, ya que es importante evitar que las células humanas escapen del riñón y se instalen en el cerebro o las gónadas del cerdo, ya sean los testículos o los ovarios, pues podría crearse un cerdo-humano.
“La cuestión es si es éticamente correcto dejar que nazcan cerdos con riñones humanizados maduros. Todo dependerá del grado de contribución [de las células humanas] en otros tejidos del cerdo”, opina el médico español que trabajó en la investigación, Miguel Ángel Esteban. Ante esto, a fin de evitar cualquier dilema ético, los expertos están modificando las células humanas para que no puedan ir al sistema nervioso central del cerdo.
Los riñones de cerdo funcionaron por 32 días

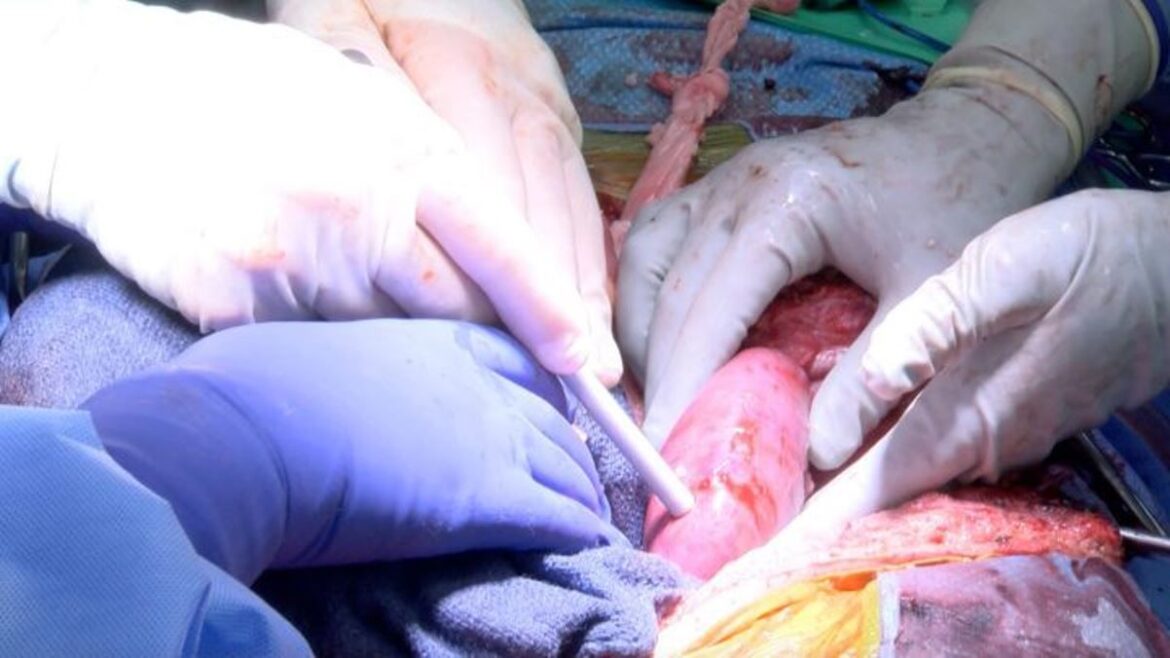
En julio de 2023, un equipo clínico del Hospital Langone Health de la Universidad de Nueva York logró trasplantar con éxito, riñones provenientes de cerdos a un hombre de 57 años con muerte cerebral que padecía enfermedad renal. El órgano alcanzó 32 días en funcionamiento que es el periodo más largo en que un riñón de cerdo modificado genéticamente, ha funcionado en un humano. Este avance sugiere que estos riñones porcinos modificados podrían ser la respuesta para aquellos pacientes en diálisis, lo que podría aliviar la falta de riñones humanos disponibles para trasplante.
Los cerdos pasaron por una modificación genética diseñada para evitar que el sistema inmunológico del receptor rechazara los nuevos órganos. Concretamente, en esta intervención, se suprimieron cuatro genes propios del cerdo que anteriormente impedían el éxito de estos trasplantes y se añadieron seis genes humanos que previenen la coagulación. Con esto “humanizan” el riñón del cerdo, evitando su rechazo, resultando en un órgano que parece más humano.
Siete días después de la operación, los análisis de sangre y las biopsias corroboraron que los riñones funcionaban adecuadamente, y que eran capaces de producir orina y procesar la creatinina. Además, no hubo evidencia de coagulación sanguínea en los órganos trasplantados, otro indicador positivo. Un informe sobre este hito fue publicado en JAMA Surgery, donde se destacó el potencial de estos xenotrasplantes o trasplantes entre especies distintas como una posible respuesta a la falta crónica de órganos humanos para trasplante.
Otros dos riñones
Este xenotrasplante viene precedido por casos como el de la Universidad de Alabama donde, en 2022, se logró el primer trasplante de dos riñones de un cerdo a un humano con muerte cerebral. Un procedimiento que demostró que los órganos funcionaron al menos durante las 77 primeras horas después de la operación.
Los riñones se extrajeron de un cerdo donante alojado en una instalación quirúrgicamente limpia y libre de patógenos. Luego se almacenaron, transportaron y procesaron para ser trasplantados.
Por otra parte, el receptor con muerte cerebral recibió la terapia estándar de inmunosupresión utilizada en un trasplante de riñón de persona a persona.
Corazón genéticamente modificado

Otro antecedente de xenotrasplante es el caso de David Bennet, primer paciente del mundo en recibir un trasplante de corazón genéticamente modificado de un cerdo, quien falleció el 8 de marzo de 2022.
Con 58 años, Bennett, quien sufría una enfermedad cardíaca terminal, sobrevivió dos meses después de la cirugía realizada en Estados Unidos. Pero su condición empezó a deteriorarse, explicaron sus médicos. El paciente estaba al tanto de los riesgos asociados con la cirugía y reconoció, antes del procedimiento, que era “un tiro a ciegas”.
Los doctores del Centro Médico de la Universidad de Maryland obtuvieron una dispensación especial del ente regulador en Estados Unidos para realizar el procedimiento, sobre la base de que el estado de Bennett – quien estaba confinado a una cama – era terminal.
“Demostró ser un paciente valiente y noble que luchó hasta el final”, dijo el cirujano que hizo el trasplante, Bartley Griffith, en un comunicado emitido por el hospital. Al respecto el médico expresó que la cirugía llevaría al mundo «un paso más cerca de resolver la crisis de escasez de órganos«.
Los xenotransplantes

Los xenotrasplantes comenzaron a explorarse a principios del siglo XX, con riñones de animales, como corderos y monos, a humanos. Sin embargo, estos intentos no tuvieron éxito, mayormente por el rechazo inmediato del órgano.
La década de 1960 fue testigo de varios intentos audaces, siendo el más famoso el trasplante de corazón de un babuino a un bebé en 1984, conocido como «Baby Fae». Aunque el bebé sobrevivió solo 20 días, el caso atrajo una atención significativa y resaltó tanto las posibilidades como los desafíos del xenotrasplante.
Una de las principales barreras ha sido el rechazo hiperagudo. Este es un proceso inmediato donde el sistema inmunológico del receptor reconoce rápidamente al órgano extraño y comienza a atacarlo. En las últimas décadas, ha habido un enfoque significativo en superar esta respuesta inmunológica.
En este sentido, durante la década de 1990 y principios de 2000, los avances en la biología molecular y la genética permitieron la creación de animales genéticamente modificados – mayormente cerdos – que poseen órganos menos propensos al rechazo. Estos animales han sido modificados para eliminar ciertas moléculas que desencadenan el rechazo hiperagudo.
Cuestión de vida o muerte
Según cifras de la Administración de Recursos y Servicios de Salud de Estados Unidos (HRSA, por sus siglas en inglés), en el mundo se trasplantan cerca de 150.000 órganos cada año, pero solo en ese país la lista de espera es de 100.000 personas, y cada día mueren 17 de ellos.
Para estos investigadores, estas innovaciones podrían evitar miles de muertes en todo el mundo por parte de aquellos que esperando para poder recibir un órgano que no llega a tiempo.
Los xenotrasplantes tienen una gran ventaja, y es que la vida media de un cerdo es de 30 años, son animales de granja que se crían fácilmente y pueden tener órganos de tamaño similar a los humanos.
La posibilidad de usar órganos de animales para satisfacer la demanda humana ha sido considerada desde hace mucho tiempo, y no suena tan descabellada si se considera que el uso de válvulas cardíacas de cerdo ya es un procedimiento médico común en algunos países. Asimismo, recientemente un equipo internacional de científicos creó una córnea a base de piel de cerdo o córnea de bioingeniería que podría devolver la vista a millones de personas.
Con información de BBC, National Geographic, Sputnik y Diario AS
No te pierdas
> Venezuela pionera en tratamientos con células madre